新冠特效药现“黑马” 中国生物入局尚存风险?
时间:2021-11-22 13:53 | 栏目:观察 | 点击:748次
出品:新浪财经上市公司研究院
作者:辰露
随着新冠疫苗市场趋于饱和,各大药企纷纷布局新冠特效药。近期全球多款新冠特效药物研发取得重大进展,人类终结疫情的话题一度引起热议。随着新冠特效药利好消息频出,越往后入局的企业越难获得较好的市场表现。
11月4日,默沙东宣布其与Ridgeback联合开发的口服药物Molnupiravir获得英国药监局批准上市,成为全球首款获批用于治疗成人轻度至中度新冠感染的抗病毒药物。
一天后,美国辉瑞制药在官网披露其研发的新冠口服药PAXLOVID临床试验结果,该药在2/3期EPIC-HR研究的中期分析中将住院或死亡风险降低了89%。消息一出,二级市场上新冠疫苗、中和抗体、检测相关板块的股价整体承压。

国内新冠特效药的研发布局也在不断推进,据《科技日报》报道称,由北京大学谢晓亮团队与丹序生物联合开发的中和抗体DXP-604已经被批准为同情用药在北京地坛医院使用,由于有高达85%的重合位点,它使得人体细胞对于新冠病毒“拒不开门”。
一线临床表现使DXP-604有望成为新冠特效药的“黑马”,其独特性在于,在其他候选药大多使用“一对抗体”预防新冠病毒逃逸时,DXP-604实现了“单个抗体”就能防范变异株。此外,单个抗体取代“抗体对”的特点使它的生产成本将不足其它候选药的三分之一,加之能防范变异株的特征,将使其在国际市场上拥有强大竞争力,成为国际制药巨头有力的竞争对手。
国内外新冠特效药竞争激烈 中国生物入局尚存风险?
值得注意的是,DXP-604目前仅作为“同情用药”使用,同情用药实际上是一种“拓展性临床试验”。按照美国食品药品监督管理局(FDA)的定义,同情用药指对于患有严重或危及生命疾病的患者,在不能通过现有药品或入选临床试验来得到有效治疗时,可以申请在临床试验之外使用未经上市许可的试验用药物。目前DXP-604还处于试验阶段,有效性安全性未知。
据报道,丹序生物已与国药集团中国生物达成合作开发意向,中国生物欲在国内市场抢先介入新冠特效药。此番布局除了要面临药物本身的风险外,还要面临国内外市场竞争。
中国生物官方公众号消息称,目前国药集团中国生物正在密集研发两款新冠治疗特效药,分别为新冠特异性免疫球蛋白和抗新冠病毒单克隆抗体。其中新冠特异性免疫球蛋白是全球第一个批准临床试验的特免产品,另一款抗新冠病毒单克隆抗体通过在体外培养表达具有高中和活性的单克隆抗体细胞(主要为CHO细胞),再经过一系列纯化步骤获得。值得注意的是,目前两款特效药均未获批上市。
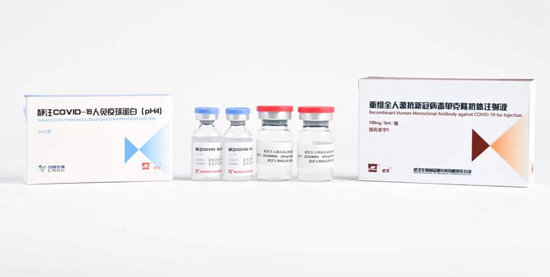
药物上市需经过严格的审批,目前全球新冠病毒有效用药的研发主要围绕阻断病毒进入细胞、抑制病毒复制、调节人体免疫系统3条技术路线开展。
Molnupiravir是一种在研的、口服形式的强效核糖核苷类似物,可抑制SARS-CoV-2(新冠病毒的致病因子)的复制。PAXLOVID是一种专门用于对抗SARS-CoV-2的3CL蛋白酶抑制剂,主要通过抑制新冠病毒3CL蛋白酶表达而阻止病毒自我复制。上述两款特效药属于第二类技术路线,而DXP-604是一种中和抗体药物,它的原型是人体里本来就有的中和抗体。在与新冠病毒过招后,患者本人的免疫机制会择优选出“会打仗”的中和抗体,属于第三类技术路线。
此外,中国生物在新冠特效药领域还面临国内外激烈的竞争。除国外制药巨头在此领域具有先发优势,国内药企也纷纷入局新冠特效药领域。
11月17日,先声药业集团(2096.HK)宣布与中国科学院上海药物研究所等就抗新型冠状病毒(SARS-CoV-2)新药开发达成项目合作。候选分子具有成为新一代口服新冠特效药的潜力,对包括德尔塔毒株在内的多种新冠变异毒株均有抑制作用。

受此消息的利好,先声药业股价应声上涨。11月18日涨13.74%。报收9.66港币/股,市值增加32.06港元。
在抗体药物方面,国内进展最快的是清华大学、深圳市第三人民医院和腾盛华创联合研发的中和抗体联合疗法。研发团队已于10月9日向国家药监局滚动提交附条件上市申报材料,有望12月底前获得批准(附条件)上市。
相比之下之下,中国生物的两款新冠特效药进度较为落后,最快的也正处于临床研究阶段,有效性安全性待确定。
一类人用疫苗产品市占率达80% 资产负债率大幅上升
中国生物成立于1919年,隶属于中国医药集团,主营业务包括人用疫苗、血液制品、医学美容、动物保健、抗体及治疗药物、医学诊断等,是我国较早布局新冠疫苗的企业之一。下辖12个二级子公司和76家二级以下子公司,拥有员工12551人。
在产品结构上,中国生物人用疫苗可年产50种,一类疫苗产品覆盖了中国免疫规划针对的15种疾病,市场占有率达80%。疫情爆发以来,中国生物一方面在筹备预防制品,另一方面备战新冠特效药。
据中国生物官方微信公众号消息,截至11月16日,中国生物已累计生产供应新冠疫苗25亿剂次,其新冠疫苗产品已在全球10个国家注册上市,112个国家、地区及国际组织批准紧急使用或市场准入,130多个国家提出明确需求,接种人群覆盖196个国别。
中国生物首席科学家张云涛公开表示,特效药固然有用,终结疫情疫苗仍是重要力量。在对抗新冠病毒的战疫中,新技术,新手段都应当被鼓励,但要彻底终结疫情,疫苗还是会发挥最重要的作用,这是对付传染病流行的真理。
随着新产品不断研发上市,近年来中国生物营收净利润均呈增长态势。据wind数据,2018-2019年及2020年前三季度,中国生物营业收入分别为108.68亿元、125.35亿元和114.05亿元,净利润分别为24.23亿元、24.27亿元和27.15亿元。
此外,截至2020年三季度,中国生物资产负债率为39.37%,较年初增长7.35个百分比。2016-2019年及2020年三季度,中国生物投资活动现金流连续四年为负,分别为-7.85亿元、-6.62亿元、-11.43亿元、-20.28亿元和-26.51亿元。
.app-kaihu-qr {text-align: center;padding: 20px 0;} .app-kaihu-qr span {font-size: 18px; line-height: 31px;display: block;} .app-kaihu-qr img {width: 170px;height: 170px;display: block;margin: 0 auto;margin-top: 10px;} 8.××%理财券,额度有限先购先得,每位用户限购一次>>